Đây là vaccine Covid-19 thứ 5 được phê duyệt tại Việt Nam, sau AstraZeneca, Sputnik V, Pfizer và Sinopharm. Vaccine này là dạng hỗn dịch tiêm bắp. Mỗi lọ chứa 10 liều, mỗi liều 0,5 ml chứa 100 mcg mRNA.
Bộ Y tế cho biết, vaccine Moderna của Mỹ nhưng có thể được sản xuất tại Tây Ban Nha, Pháp, căn cứ vào khả năng cung cấp vaccine tại thời điểm nhập khẩu nộp hồ sơ đề nghị cấp phép.
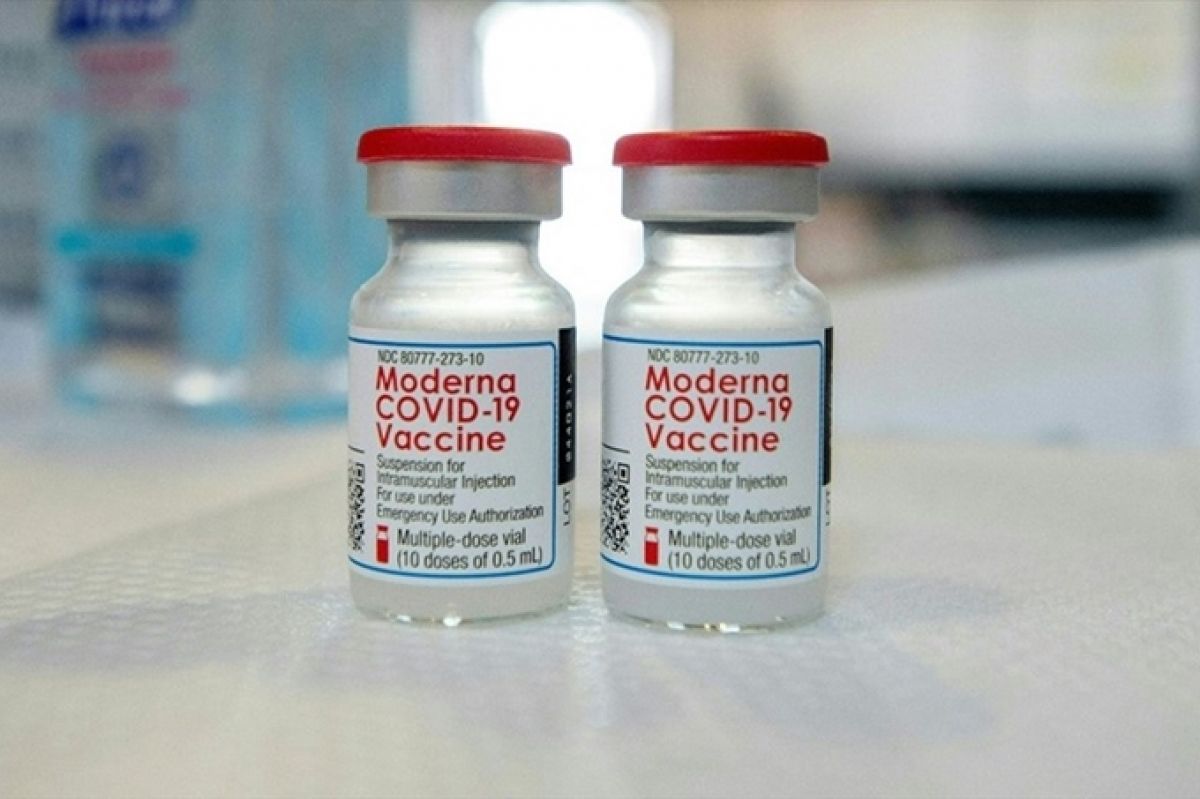
Tại Việt Nam, Tập đoàn Zuellig Pharma là đơn vị chịu trách nhiệm phân phối vaccine Moderna.
Vaccine Spikevax được phê duyệt dựa trên dữ liệu an toàn, chất lượng và hiệu quả do Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam cung cấp cho Bộ Y tế Việt Nam tính đến ngày 23/6/2021 và cam kết của Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam về tính chính xác của các tài liệu đã cung cấp cho Bộ Y tế Việt Nam.
Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam có trách nhiệm phối hợp với cơ sở sản xuất vaccine phản hồi kịp thời các yêu cầu từ Bộ Y tế Việt Nam để bổ sung thêm dữ liệu hoặc các yêu cầu khác có liên quan đến vaccine Spikevax và chủ động cung cấp, cập nhật các thông tin mới có liên quan đến vaccine Spikevax cho Bộ Y tế Việt Nam trong suốt quá trình phát triển sản phẩm;
Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam chịu trách nhiệm phối hợp với cơ sở sản xuất vaccine đảm bảo các điều kiện sản xuất tại cơ sở sản xuất vaccine Spikevax nhập khẩu vào Việt Nam và đảm bảo an toàn, hiệu quả và chất lượng của lô vaccine Spikevax nhập khẩu vào Việt Nam; Phối hợp với đơn vị phân phối, sử dụng vaccine Spikevax triển khai hệ thống cảnh giác dược toàn diện đối với vaccine này tại Việt Nam theo quy định của pháp luật;
Phối hợp với Cục Khoa học công nghệ và Đào tạo và đơn vị có đủ điều kiện tổ chức thực hiện việc đánh giá tính an toàn, hiệu quả của vaccine Spikevax trên cơ sở ý kiến tư vấn của Hội đồng tư vấn sử dụng vaccine, sinh phẩm y tế của Bộ Y tế trong quá trình sử dụng;
Phối hợp với Viện Kiểm định Quốc gia vaccine và sinh phẩm y tế trong việc kiểm định các lô vaccine Spikevax trước khi đưa ra sử dụng; phối hợp với Cục Y tế dự phòng hướng dẫn việc bảo quản, phân phối và sử dụng vaccine Spikevax cho các cơ sơ tiêm chủng.
Bộ Y tế cũng yêu cầu Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam phải phối hợp với Bộ Y tế Việt Nam để triển khai quản trị rủi ro đối với vaccine Spikevax trong suốt quá trình lưu hành tại Việt Nam. Đồng thời, việc sử dụng vaccine Spikevax phải theo hướng dẫn của Bộ Y tế Việt Nam./.


